

アルツハイマー型認知症 (AD) は、認知症を発症する疾患の中で最も患者の数が多く、国内に約200万人存在するとされており、高齢化社会が進むにつれ、その数は増加していくものと考えられています。
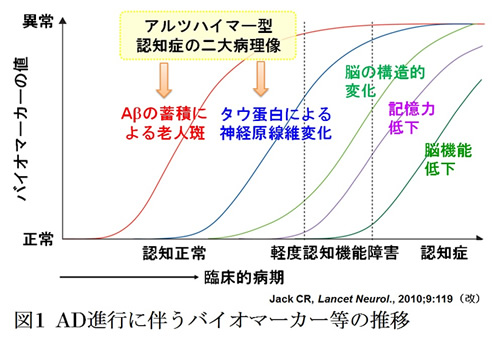
図1はAD進行に伴うバイオマーカー (生物学的指標) 等の推移を示しています。
右に行くほど重度の症状になります。医療機関でADと診断される時はすでに脳機能が低下していることが多く、症状の進行を遅らせる薬剤を服用しても、生活の質の劇的な向上は期待できません。そのため、より早期の段階でAD発症の可能性を判別することが重要となります。
その早期段階のバイオマーカーとして、アミロイドβタンパク質(Aβ) と、過剰にリン酸化されたタウ蛋白質が挙げられます。特に、Aβは細胞毒性を有する老人斑の主要構成成分であり、AD発症の20年ほど前から徐々に蓄積し、神経細胞を脱落させADに至ります。そのため、Aβに集積する薬剤を用いて脳内のAβ蓄積量を画像化できれば、AD発症の予測が可能となります。これをアミロイドイメージングと呼びます。実際にはAβに集積する薬剤を、F-18やC-11のようなPETで利用する放射性核種で標識しておき、投与された薬剤の集積部位をPETカメラで非侵襲的に検出するという手法です。
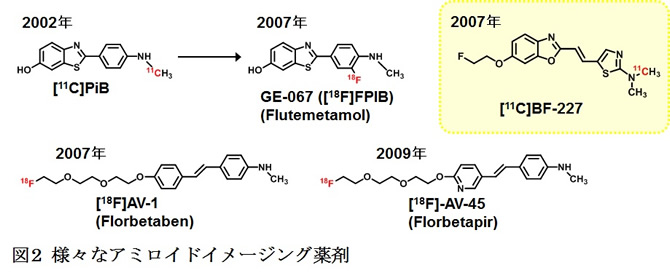
代表的なアミロイドイメージング薬剤には、C-11標識製剤の[11C]PiB、[11C]BF-227、F-18標識製剤の[18F]FPIB、[18F]AV-1, 45等が挙げられ (図2)、いずれもAD診断に対して有用性が確認されています。このうち[11C]BF-227は、2007年にBF研究所と東北大学により開発された唯一の日本製薬剤で、現在、探索的臨床研究へと展開されています。
[11C]BF-227より以前に開発された[11C]PiBによるアミロイドイメージングでは、陽性と診断された軽度認知障害の患者は、1年後に25%が、3年後には80%がADを発症しています。一方、陰性と診断された軽度認知障害の患者では、AD発症が確認されないことが報告されています。これは、アミロイドイメージングによって陽性と診断されると、高い確率でADを発症することを予測できる一方、陽性と診断されても、ADを発症しない、あるいは、他の認知症に進行する可能性を示しています。[11C]BF-227は、パーキンソン病やレビー小体型認知症の要因物質であるα-シヌクレインという蛋白質との親和性も保有しており、AD以外の認知症発症の予測も期待できるといった長所を持ち合わせています。
現在、ADの信頼性の高い診断には、脳脊髄液中のAβの減少、リン酸化タウ蛋白質の増加を調べる検査が挙げられますが、これらの検査は侵襲的であり、健診には不向きです。したがって、認知症診断検査の評価やMRI、CTの所見、遺伝子変異の有無、脳波等に加え、FDG-PETの結果も組み合わせた上での、総合的な判断が求められています。
当施設では、平成24年度より、大阪大学と共同研究を行い、[11C]BF-227の臨床利用に向けて、当施設での最適な調製法確立に取り組んでいます。
詳しくは当センターまでお問い合わせください。